HPC und KI im Einsatz für Bilderkennung und Simulation in der Systembiologie Zusehen und verstehen, wie sich Leben entwickelt
Künstliche Intelligenz und HPC helfen Systembiologen in Dresden bei der Forschung und Visualisierung. Ivo Sbalzarini und sein Team haben am Center for Systems Biology Dresden (CSBD) des Max-Planck-Instituts für Molekulare Zellbiologie und Genetik (MPI-CBG) und der Technischen Universität Dresden ein IT-Framework mit neuer Beschreibungssprache für Algorithmen entwickelt. Der Professor hat sein Projekt auf der ISC 2019 in Frankfurt/Main vorgestellt.
Anbieter zum Thema
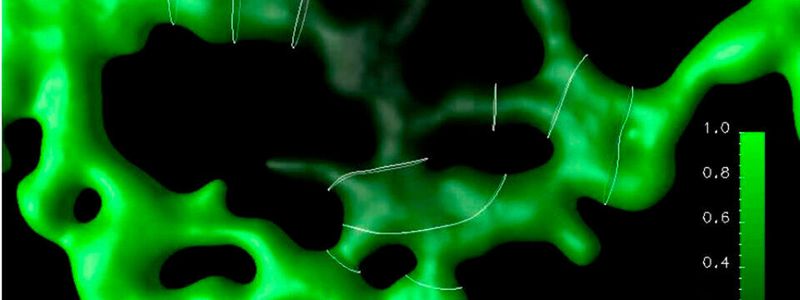
Computer-basierte Biologie erforscht biologische Zellsysteme mithilfe von Rechnern. Damit sie optimal auf biologische Phänomene abgestimmt werden können, ist die Entwicklung neuartiger numerischer und berechnender Methoden (Algorithmen) nötig.
Berechnende Biologie sieht sich zahlreichen Herausforderungen gegenüber, von komplexen geometrischen Formen bis zu ungleichmäßigen Prozessen. „Wir entwickeln und applizieren Methoden in einem zielgerichteten, Team-basierten Design-Ansatz mit dem Ziel, algorithmisch zu verstehen, wie Zellen Gewebe bilden“, schreibt Sbalzarini, Lehrstuhlinhaber für Wissenschaftliches Rechnen in der Systembiologie an der Fakultät Informatik der Technischen Universität Dresden (siehe:. „Scientific Computing for Image-based Systems Biology“).
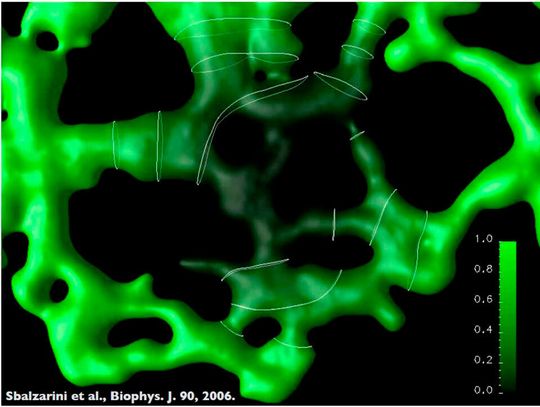
Die Algorithmen, welche innerhalb lebender Zellen bei der Gewebebildung ablaufen, bestimmen, in welche Richtung eine Zelle in einem Organ sich entwickelt, teilt oder bewegt. Zellen „berechnen“ die Antwort anhand verschiedener Faktoren und Signale aus der Umgebung, aber mit welchen Mitteln und nach welchen Maßgaben, ist unbekannt. Geht diese Berechnung schief, so entsteht ein Zellhaufen oder ein bösartiger Tumor, also Krebs. Dieser und anderen wichtigen Fragen geht Sbalzarinis Institut nach.
Der Forschungsprozess stellt sich auf den Kopf
Zellen in einem Gewebe werden als „ausgefeiltes stochastisches, paralleles Rechengerät“ betrachtet. Während die Hardware-Komponenten (Moleküle) und der Quellcode (DNS, Genom) relativ gut bekannt sind, trifft dies auf die Algorithmen nicht zu.

Ziel ist es, diese Algorithmen durch Reverse-Engineering der frühen Embryonalentwicklung von drei Arten (Fadenwurm, Fruchtfliege und Zebrafisch zu entdecken. Es geht also um nichts Geringeres, als die embryonale Gewebeformung virtuell im Rechner zu simulieren.
Dieses Vorhaben erforderte die inzwischen erfolgte Entwicklung eines Paradigmas für die mehrskalige Simulation biologischer Prozesse sowie von interaktiver Mikroskopie in Echtzeit. In technischer Hinsicht machte das Projekt Fortschritte in HPC sowie in den entsprechenden Programmiersprachen notwendig.
KI und natürlichsprachige Algorithmen
„Vor dem Hintergrund von Theorie, Algorithmen, Software und Anwendung konzentrieren wir uns in unserem Team auf bestimmte Methoden, die von bildgebender Systembiologie benötigt werden“, so Sbalzarini.
- 1. Adaptive Simulationsmethoden mit unterschiedlicher Auflösung, die Partikel verwenden, um auf numerische Weise partielle Differentialgleichungen auf komplexen dreidimensionalen Geometrien und Oberflächen zu lösen;
- 2. Bildverarbeitung und -analyse mithilfe von Partikelmethoden für die Segmentierung und Bewegungsverfolgung in Bildern aus Fluoreszenzmikroskopie;
- 3. Paralleles HPC für Partikelmethoden und hybride Partikel-Gitter-Methoden, sowie deren Softwareprogrammierung;
- 4. Biologisch inspirierte Algorithmen für Optimierung und datengetriebenes Lernen biologischer Modelle.
Bislang hat die Forschergruppe drei Simulationsmodule entwickelt. Um die Simulationen jeweils mit den Beobachtungen im Mikroskop vergleichen zu können, sind Korrelationen in Echtzeit nötig.

Entspricht die Vorhersage der Simulation dem beobachteten Ergebnis? Falls nicht, müssen die Parameter des Modells optimiert werden – natürlich in 3D und in Echtzeit. Mittelfristig soll eine gestengesteuerte VR-Visualisierung der 3D-Mikroskopie und der Simulationsergebnisse realisiert werden. Die entsprechende, neue Bildgebung ist sehr anspruchsvoll.
Für die Bildanalyse hat die Forschergruppe bereits die Software Mosaik-Suite Software veröffentlicht, die weltweit nach eigenen Angaben von 2017 ungefähr 3.000 Mal pro Monat heruntergeladen wird.
Paralleles HPC für Systembiologie
Für die Visualisierung werden GPUs verwendet, für Bildanalyse und Simulationen HPC-Cluster. In der Kombination ist eine HPC-Umgebung für Partikelmethoden entstanden.
In ihr wird seit 2005 die Softwarebibliothek Parallel Particle Mesh (PPM) ausgeführt. Diese PPM-Library hat nach Sbalzarinis Angaben einige der umfangreichsten und effizientesten Simulationen ermöglicht und die Dauer für die Code-Entwicklung von Jahren auf Wochen verkürzt. In 2019 wurde PPM durch einen modernen C++-Nachfolger, OpenFPM, ersetzt.
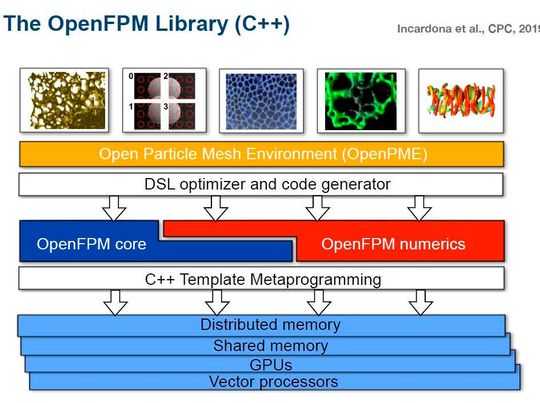
Für ihre Simulationen hat das Team zudem mit „PPME“ eine anwendungsspezifische Programmiersprache entwickelt. Mithilfe von PPME kann das Team binnen weniger Stunden sowohl eine parallel ausgeführte, skalierbare Partikelmethode für eine Simulation als auch Bildverarbeitung auf die Beine stellen.
Auf der Suche nach Synergien
Zuvor kostete es Jahre, um solchen Code von Hand zu parallelisieren. Bei der Bildverarbeitung erlauben OpenFPM und PPME in Echtzeit die Bildsegmentierung noch während eine Aufnahme mit dem Mikroskop erfolgt (siehe: A Parallel Distributed-Memory Particle Method Enables Acquisition-Rate Segmentation of Large Fluorescence Microscopy Images).
Um von Synergien in der Entwicklung von Software zu profitieren, nimmt das Team am "Dresden Software Synergy Consortium" teil und trägt zu Opensource-Projekten wie „ImageJ2“ und „Fiji“ für die Bildverarbeitung sowie „ClearVolume “ für die Echtzeit-3D-Mikroskopie und „Scenery“ für die VR-Visualisierung großer Daten bei. Zudem stellt es seine Methoden als wiederverwendbare Workflows zur Verfügung. Sämtlicher Quellcode ist auf öffentlichen Git-Servern zu finden.
Artikelfiles und Artikellinks
(ID:46110071)




:quality(80)/p7i.vogel.de/wcms/7c/52/7c5227112fa05f60e21a5880ef9e5b6b/0130929467v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/0c/b6/0cb659b857a730ab94b3641fb3932da5/0130793406v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/63/c4/63c4700dcf2d980c5a5c4ed41890c62b/0130812458v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/cc/65/cc65db9a62526f90292fb2fb1212b524/0130698558v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/23/5a/235a7cc8f0f6ee6992d706dd2422bb1f/0130911332v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/49/7a/497af014bb9c80eb964cbd4b170f1af6/0130709118v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/2c/11/2c11353be10b8aff5cfc4c83246199e9/0130640586v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/30/eb/30eb9324ea3126096eb3a2ef820a8be5/0130704464v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/d9/e4/d9e4f7b94025360fa28245bfccc07ada/0130927746v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ad/ec/adec05b770cd908c372d6641faf88fa1/0130765706v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/ae/f9/aef9cef6337f8d1593202170a319e812/0130764658v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/42/ff/42ff4fc17a11a3fa7065cefc168ef25d/0130824377v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ac/4d/ac4d77a2d88556f01607b93d63a25f3e/0130721386v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/bf/d3/bfd3a10ee878513bdf4c27db38128ed0/0130670809v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/ad/e9/ade9d0a11085d64eaaacbe51d683beca/0130726498v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/e7/b3/e7b349f9bb427752fd3f4ae4c52c957d/0130852653v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/81/b3/81b359118a0e0e395cdebbddcfa03243/0130668020v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/93/91/9391c9624ce4cfd414eaed171c3e50b8/0130668778v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/4b/52/4b528e4b495a537cda6df2ae3eee775e/0130637010v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/73/62/7362883dfa5efc0dcacb2e148a5dd7e0/0130738599v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/8f/52/8f52fcd16c1c96d52b39995b962f135e/0130846855v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/8a/ba/8abadeb121d645fdb8fb5a68d6a4c9b8/0130541481v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/c4/43/c44345288e65c7a41cd5ce0da355ba1f/0130874335v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/82/7c/827c5f9c44ee0352eb65cb7165c5c1ec/0130754825v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/39/09/39092db30c8b2ac9fe8f597982708ccd/0130670623v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/f3/da/f3dacd38e5834ae3f3c9d0a4bc9664d3/0113348475.jpeg)
:quality(80)/p7i.vogel.de/wcms/90/f5/90f56ec6cb3ddbdabca2162fd5477836/0113078524.jpeg)
:quality(80)/p7i.vogel.de/wcms/0f/09/0f097990002b7600075e43c92af4a3fd/0110524571.jpeg)
:quality(80)/p7i.vogel.de/wcms/66/ae/66ae9e32738784b57e2ad8c1a4b0986f/0109756744.jpeg)
:quality(80)/p7i.vogel.de/wcms/00/24/0024808d38d25431ae2719d3f8252908/0130726727v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/21/1c/211c24358dafb0b5433509e917e532b3/0130567036v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/5c/1e/5c1e606e8d54467bc29043a16a344dd7/0130157161v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/ee/3f/ee3f063b82737f0369c09ba7854587b5/0127234708v1.jpeg)
:quality(80)/p7i.vogel.de/wcms/f1/f0/f1f007a4518fa65d3cb0ea5ca465142a/0121300054v3.jpeg)
:quality(80)/p7i.vogel.de/wcms/a8/28/a828f76369267628d833a12c26dd6579/0121131534v3.jpeg)
:fill(fff,0)/p7i.vogel.de/companies/68/f7/68f771f60cae6/kentix-logo-endorsed-colored-rgb.png)
:fill(fff,0)/p7i.vogel.de/companies/60/2a/602a8645d40e9/200226---derz-logo.jpg)
:quality(80)/p7i.vogel.de/wcms/f1/95/f1950d4a88c49d395daa5e49e85e93da/0130054266v2.jpeg)
:quality(80)/p7i.vogel.de/wcms/7f/39/7f3904c8e34848303d65dcb8fa84bef0/0126326548v1.jpeg)